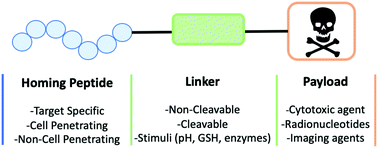
على الرغم من التقدم المستمر في العلاج بالأجسام المضادة والأدوية المتقارنة (ADCs)، لا تزال هناك العديد من التحديات. على سبيل المثال، يؤدي الهيكل المعقد للـ ADCs إلى ارتفاع تكاليف الإنتاج وعمر نصف طويل، مما يزيد من السمية الجهازية بسبب التعرض لفترة طويلة في البلازما. ونتيجة لذلك، برزت مترافقات الببتيد والمخدرات (PDCs) كبديل واعد. تتكون PDCs من ثلاثة مكونات: الببتيد الموجه، والرابط، ودواء الحمولة. ومن خلال الاستفادة من التقارب العالي للببتيدات الموجهة لمستقبلات سطح الورم، تقوم الخلايا PDC بتوصيل دواء الحمولة مباشرة إلى الهدف.

نماذج حمولات PDC
يمكن أن تحمل أجهزة PDC أشكالًا مختلفة من الحمولات. يمكن أن تكون هذه أدوية العلاج الكيميائي التقليدية مثل باكليتاكسيل أو جيمسيتابين. تُستخدم النظائر المشعة أيضًا في التشخيص الدقيق للأمراض والعلاج الإشعاعي المستهدف. تشمل النظائر التشخيصية الفلور -18 (18F)، والنحاس -64 (64Cu)، والجاليوم -68 (68Ga)، واليود -123 (123I). ترتبط هذه النظائر، المقترنة باستهداف الببتيدات، بمستقبلات الخلايا السرطانية، مما يتيح توطين الأنسجة الخبيثة بدقة من خلال الكشف عن البوزيترونات الصادرة عن النظائر. عندما ترتبط الببتيدات المستهدفة بالنظائر المشعة مثل الإنديوم-111 (111In)، والإيتريوم-90 (90Y)، واللوتيتيوم-177 (177Lu)، تعمل PDCs كعوامل علاج إشعاعي مستهدفة. تشمل الحمولات الأخرى لـ PDCs البروتينات والأجسام المضادة والببتيدات والأحماض النووية.

مزايا PDC
تقدم PDCs أوجه تشابه مع ADCs ولكنها تتغلب على بعض القيود الخاصة بها. بالمقارنة مع ADCs، تتمتع PDCs بوزن جزيئي أصغر، وتغلغل أفضل للأنسجة، ومناعة أقل أو معدومة. علاوة على ذلك، تعد مركبات PDC أسهل في التوليف والتنقية والتعرف، مما يؤدي إلى انخفاض تكاليف الإنتاج. مع التقدم في تكنولوجيا التدوير، وتقنية عرض العاثيات، وتقنية عرض mRNA لاستهداف اختيار الببتيد، تسارع تطوير أدوية PDC. من المتوقع أن تصبح PDCs الجيل التالي من الأدوية المستهدفة بعد الأدوية المستهدفة للجزيئات الصغيرة، وأدوية الأجسام المضادة، وADCs.
الخصائص الدوائية لل PDCs
امتصاصتتمتع PDCs بوزن جزيئي كبير نسبيًا ونفاذية ضعيفة مقارنة بالجزيئات الصغيرة التقليدية. نظرًا لعدم استقرار الببتيدات في الجهاز الهضمي، يتم إعطاء الـ PDCs الحالية في السوق وفي المراحل السريرية عن طريق الوريد، متجاوزة عملية الامتصاص. ويمكن أيضا أن تدار تحت الجلد أو في العضل، وتدخل مجرى الدم أو الجهاز اللمفاوي. من العيوب الكبيرة للـ PDCs كأدوية هو عدم استقرارها وقصر نصف عمرها في الجسم الحي، حيث تتحلل الببتيدات بسرعة بواسطة البروتياز ويتم التخلص منها بسهولة عن طريق الكلى. وهذا يمثل مشكلة خاصة في علاج الأورام الصلبة، حيث تكون الدورة الدموية الموسعة ضرورية لاختراق أنسجة الورم بشكل مناسب. يعد تعديل الببتيدات لتعزيز الاستقرار وإطالة عمر النصف استراتيجية حاسمة.
توزيعيتم تصنيف الببتيدات PDC إلى نوعين: الببتيدات المستهدفة للخلايا (CTPs) والببتيدات المخترقة للخلايا (CPPs). نظرًا لانخفاض خصوصية CPPs للخلايا، لا يتم استخدامها بشكل عام كببتيدات موجهة في PDCs. تستهدف الخلايا PDC الأورام بطريقتين: 1) ترتبط الخلايا PDC بالمستقبلات المفرطة التعبير على أسطح الخلايا السرطانية، وتدخل الخلايا عن طريق الالتقام الخلوي، وتطلق السموم في الليزوزومات؛ 2) تطلق الخلايا السرطانية PDC السموم في بيئة الورم، والتي تدخل بعد ذلك إلى الخلايا السرطانية وتقتلها.
الاسْتِقْلابيتم استقلاب PDCs في الجسم الحي عبر ثلاثة مسارات رئيسية:
- التخلص من المخدرات عبر الهدف (TMDD): TMDD هو مسار التخلص المحدد. ترتبط الخلايا PDC بمستقبلات على الخلايا المستهدفة، ويتم استيعابها، وتتحلل إلى أحماض أمينية وببتيدات في الليزوزومات. ومع ذلك، عادة ما يكون عدد الأهداف على أسطح الخلايا محدودًا، مما يجعل TMDD قابلاً للإشباع ويؤدي إلى حركية دوائية غير خطية.
- التمثيل الغذائي غير النوعي: يمكن للعمليات غير المستهدفة مثل التحلل البروتيني واحتساء الخلايا غير النوعي أن تطلق سمومًا خلوية جزيئية صغيرة في مواقع غير مقصودة، مما يسبب آثارًا جانبية خارج الهدف.
- المناعة: قد تؤدي الـ PDCs إلى تحفيز المناعة، مما يحفز إنتاج الأجسام المضادة للأدوية (ADAs)، التي تحيد الدواء وتشكل مجمعات يتم تطهيرها بواسطة الجهاز المناعي. من المهم أن نلاحظ أن الاستجابات المناعية أو ADA التي لوحظت في الحيوانات قبل السريرية لا تتنبأ باستجابات ADA البشرية.
إفرازتتم إزالة PDCs، ذات الوزن الجزيئي الأصغر بكثير من عتبة الترشيح الكلوي (60 كيلو دالتون)، بسرعة عن طريق الكلى، مما يمنع التراكم الفعال للسموم الخلوية في الأورام. لذلك، تعد التعديلات أو التعديلات الكيميائية على الببتيدات الموجهة للـ PDCs ضرورية لتعزيز الاستقرار وإطالة عمر النصف. قد يكون الإفراز الكلوي هو طريق التصفية الأساسي لبعض الببتيدات أو أدوية PDC. في مثل هذه الحالات، من الأهمية بمكان مراعاة أن معدل التصفية المحسوب من التحليل غير المجزأ (NCA) بعد إعطاء الدواء الرابع يجب أن يشير إلى معدل الترشيح الكبيبي للدواء بدلاً من تدفق الدم الكبدي.
استراتيجيات دراسة الحركية الدوائية للـ PDCs
تستخدم PDCs بطبيعتها استراتيجيات الاستهداف لتوصيل الأدوية، وتجمع بين خصائص كل من الأدوية الجزيئية الكبيرة والصغيرة. ونظرًا لعدم الاستقرار النسبي ومشكلات الاستهداف، فإن السمية المحتملة للحمولة تتطلب اهتمامًا خاصًا. في مرحلة فحص الأدوية، تركز دراسات DMPK على تحسين استقرار الببتيدات وPDCs في الدم الكامل والبلازما والمتجانس الكلوي، مع الاستمرار في تحسين بنية PDC من خلال تحديد المستقلبات في المختبر وفي الجسم الحي لتعزيز الاستقرار ونصف العمر. يوصى بإجراء دراسات توزيع الأنسجة على القوارض في وقت مبكر من المشروع لتقييم السمية المحتملة للحمولة على الأعضاء المختلفة.
في مرحلة المرشح السريري، ينبغي تحديد النماذج المناسبة في المختبر لتقييم والتحقق من صحة إطلاق الحمولة في الجسم الحي. ينبغي للتجارب في الجسم الحي قياس تركيز الدم من PDC والحمولة في وقت واحد. في ظل ظروف الجرعات المتكررة، من المستحسن مراقبة تأثيرات ADA. من الضروري إجراء تجارب توزيع الأنسجة في أنواع PD لتقييم قدرة استهداف PDCs.
الاستنتاج والتوقعات
على الرغم من الخبرة الواسعة في تطوير أدوية ADC، فإن تطوير أدوية PDC ليس طريقًا مباشرًا ولكنه مليء بالفرص والتحديات. بالمقارنة مع ADCs، فإن خصوصية الأنسجة واستهداف الورم للببتيدات أقل شأناً إلى حد ما، مما يشكل تحديات كبيرة لاختيار الببتيدات المستهدفة. بالإضافة إلى ذلك، بسبب ضعف استقرار الببتيدات، فإن تناوله عن طريق الفم يمثل صعوبة كبيرة. تواجه الشركات المساهمة العامة أيضًا تحديات تحليلية وتأثيرات محتملة خارج الهدف.
يدمج تصميم أدوية PDC مزايا استهداف الببتيدات وأنواع مختلفة من الأدوية. إن الموافقات التنظيمية الأخيرة للأدوية العلاجية والنويدات المشعة وعوامل التشخيص تسلط الضوء على إمكانات هذه الأدوية. إن تشجيع النتائج السريرية من خلال خطوط الأنابيب السريرية المستمرة يؤكد بشكل أكبر على وعدهم. من خلال اقتران مختلف الكيانات الجزيئية واستهداف الببتيدات، فإن تطوير أدوية PDC يحمل إمكانات كبيرة للمستقبل.